近日,3499cc拉斯维加斯入口何玲/孙逸团队联合海军军医大学庄春林团队在生命科学学科顶尖期刊Redox Biology (IF:11.4)发表最新研究论文:A potent phosphodiester Keap1-Nrf2 protein-protein interaction inhibitor as the efficient treatment of Alzheimer’s disease。3499cc拉斯维加斯入口孙逸老师为共同第一作者(排一),3499cc拉斯维加斯入口何玲教授和海军军医大学庄春林教授为本文共同通讯作者。我校为第一通讯单位。
阿尔兹海默症(Alzheimer’s disease, AD)已经成为全球重点关注的公众健康问题,但其发病机制尚不明确,药物研发的难度极大。近些年,在研究AD的过程中,越来越多的研究者把目光投向了核因子E2相关因子2(Nuclear factor erythroid 2-related factor 2, Nrf2)。多项临床及动物实验表明Nrf2是认知功能障碍发生发展的关键靶点之一。2017年起,团队成员相互合作,围绕Keap1-Nrf2蛋白-蛋白相互作用抑制剂,开展了一系列关于AD的病理机制和药理研究。前期设计筛选得到化合物NXPZ-2,不仅具有优异的体外抑制活性,并且在双侧海马立体定位注射Aβ寡聚体建立AD小鼠模型中也表现出对小鼠学习、探索、空间记忆等认知功能的明显改善作用,甚至显著优于阳性对照多奈哌齐。进一步机制研究显示,给药后AD小鼠神经元数量恢复,相关AD 标志蛋白减少。并且化合物能够促进Keap1-Nrf2解离,Nrf2入核增多,脑内抗氧化能力增强。相关研究结果发表于Bioorg Chem杂志。在此基础上,通过基于结构、基于片段的药物设计技术,优化各个关键位点,开展系统构效关系研究,获得高活性化合物POZL。晶体学研究证明POZL与人Keap1-Kelch 结构域2.7Å分辨率的晶体之间存在强相互作用。动物在体及原代神经元离体研究进一步证明POZL可通过调控Keap1-Nrf2-AREs信号通路抑制中枢神经系统的氧化应激反应实现神经元保护作用,通过调控BACE1和NDP52的表达实现对AD病理蛋白Aβ及P-tau的抑制作用,改善突触功能,进而显著改善APP/PS1转基因AD模型小鼠的认知障碍。研究成果可为POZL作为AD治疗药物的研发和临床应用提供理论指导和实验依据。
以上工作获得国家自然科学基金、宁夏自治区重点研发计划(重点项目)等项目资助。
论文链接:
https://www.sciencedirect.com/science/article/pii/S2213231723001945?via%3Dihub
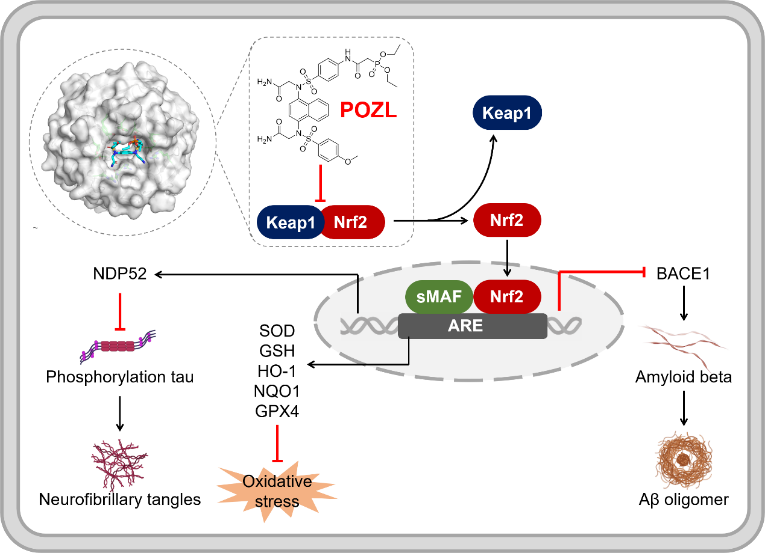
示意图
(供稿单位:3499cc拉斯维加斯入口,撰写人:刘华)





