近日,我校3499cc拉斯维加斯入口周建平、丁杨团队在国际著名期刊Advanced Science(IF= 16.806),Nano Letters(IF =11.189)以及Journal of Controlled Released(IF= 9.776)相继发表了阿尔兹海默症治疗的最新系列研究成果。
基于阿尔兹海默症(AD)病理机制和血脑屏障(BBB)药物渗透限制,该团队全面总结了近年来靶向阻断AD疾病进程的纳米药物应用进展,并探讨了以病理机制指导的纳米药物设计原则(图1)。相关工作以“Versatile nanomaterials for Alzheimer's disease: Pathogenesis inspired disease-modifying therapy”为题发表在Journal of Controlled Release上。2021级直博生习艺龙和2020级硕士生陈赟为本文共同第一作者,我校周建平教授、丁杨副教授、张华清博士后为本文共同通讯作者,我校为本文的唯一通讯单位。(全文链接:https://doi.org/10.1016/j.jconrel.2022.02.034)
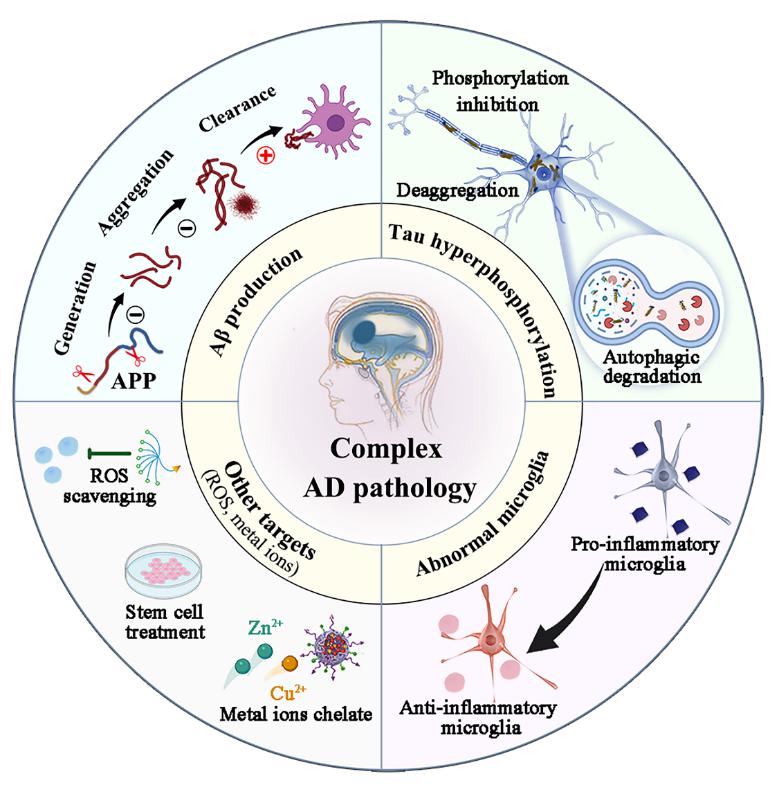
图1 基于AD病理机制及关键靶点的抗AD纳米药物开发策略示意图。
针对脑内β淀粉样蛋白(Aβ)代谢异常和小胶质细胞功能障碍之间的“炎性恶性循环”,该团队构建“三位一体”式脂蛋白纳米清道夫,以实现载体加速小胶质细胞清除Aβ,姜黄素抑制小胶质细胞炎症和siBACE1基因沉默减少神经元的Aβ的“全链式”AD治疗(图2)。该工作基于AD中小胶质细胞的“双刃剑”病理角色,提出针对小胶质细胞源性神经炎症的“三位一体”调控策略,为AD治疗提供了新思路和新方案。相关工作以“Lipoprotein-Inspired Nanoscavenger for the Three-Pronged Modulation of Microglia-Derived Neuroinflammation in Alzheimer’s Disease Therapy”发表在Nano Letters上。博士后张华清、硕士研究生江文心和赵元培为本文共同第一作者,我校周建平教授、丁杨副教授为本文共同通讯作者,我校为本文的唯一通讯单位。(全文链接:https://pubs.acs.org/doi/10.1021/acs.nanolett.2c00191)
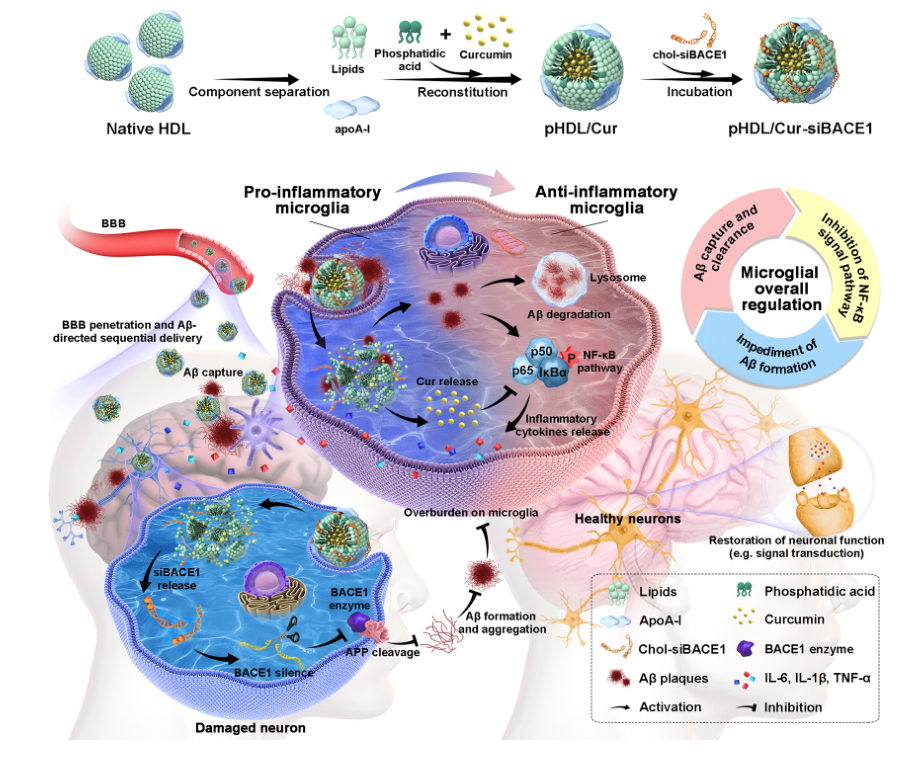
图2 pHDL/Cur-siBACE1的制备与“全链式”AD治疗示意图。
针对AD病变的两大关键诱因:β淀粉样蛋白(Aβ)沉积和Tau蛋白过度磷酸化,该团队以天然高密度脂蛋白活性组分载脂蛋白A-I和磷脂仿生组装Aβ高亲和纳米复合物,并荷载Tau蛋白磷酸化抑制剂亚甲蓝;为高效渗透入脑,经模拟肽仿生锚定并优化靶向配体密度,构建“药物-载体”协同治疗组装体;在AD病灶,载体捕获Aβ入小胶质细胞高效清除;药物借助载体实现神经元胞内富集,抑制Tau磷酸化和聚集,实现针对Aβ和Tau双病理的“药物-载体”协同治疗(图3)。相关成果以题为““Drug-Carrier” Synergy Therapy for Amyloid-β Clearance and Inhibition of Tau Phosphorylation via Biomimetic Lipid Nanocomposite Assembly”发表于Advanced Science(全文链接:https://doi.org/10.1002/advs.202106072)。2020级博士研究生韩国臣和2021级硕士研究生白凯文为本文共同第一作者,我校周建平教授、丁杨副教授、张华清博士后为本文共同通讯作者,我校为本文的唯一通讯单位。
以上研究工作得到了国家和省级自然科学基金、中国博士后科学基金、江苏省博士后项目、江苏省高校重点学科发展基金等资助。
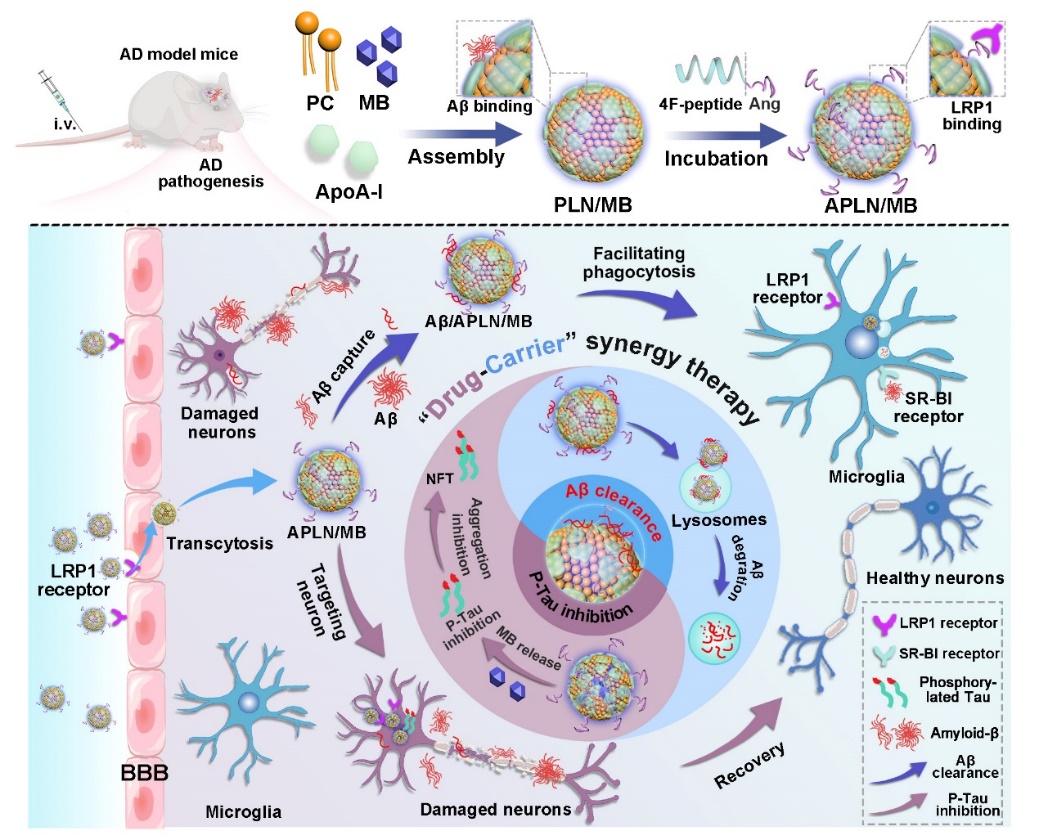
图3 仿生脂质纳米复合物组装体APLN/MB制备过程及其治疗示意图。
(供稿单位:3499cc拉斯维加斯入口,撰写人:姜红,审稿人:吴旻玥)





