近日,共识一流期刊Cell Metabolism杂志在线发表了我校郝海平教授团队题为Psychological Stress-induced Microbial Metabolite Indole-3-acetate Disrupts Intestinal Cell Lineage Commitment的最新研究成果。该研究揭示了慢性精神应激诱导肠上皮细胞损伤易感性的脑-肠信号传递与代谢调控新机制,并发现了具有临床监测应用价值的菌群代谢标志物。我校3499cc拉斯维加斯入口博士生魏崴、硕士毕业生刘雅利以及博士后侯园龙为本文的共同第一作者,郝海平教授、王广基院士、郑啸教授与东南大学袁勇贵教授为共同通讯作者,我校为论文第一通讯单位。该论文被Cell Metabolism杂志选为3月刊封面文章,同时,Nature主页以NEWs的形式对该研究进展进行了同步报道。
流行病学研究表明,长期暴露于精神心理压力会驱动多种疾病的发生发展。例如,现代社会慢性精神心理压力与炎症性肠病、肠易激综合征等肠道疾病高发密切相关。然而,目前人们对于精神应激下脑-肠双向信号传递机制,特别是心理压力如何传递并扰动肠道内稳态仍然知之甚少。围绕以上问题,郝海平教授团队基于前期建立的慢性束缚应激小鼠模型及足底电击模型,发现慢性心理压力暴露会引发不可逆的小肠上皮细胞功能紊乱。通过类器官培养、肠干细胞分化谱系示踪及多组学方法,团队发现以上表型与精神应激下小肠干细胞(ISC)线粒体生物能和功能稳态破坏有关。团队进一步通过化学干预、无菌小鼠、代谢组学及工程菌构建等实验手段发现鼠乳杆菌(L. murinus) 及代谢物吲哚-3-乙酸(IAA)在应激诱导的ISC谱系分化异常中发挥关键作用。后续机制研究表明IAA作为代谢信号抑制ISC线粒体生物能从而以细胞固有的方式破坏其谱系分化、加重肠上皮细胞损伤,而补充三羧酸循环中间体α-酮戊二酸可有效挽救IAA 诱导的体内外损伤。最后,研究团队在患有不同精神困扰的临床患者中证实精神应激下肠道菌群IAA产生能力持续增加并与肠道功能障碍相关。
该研究通过多学科技术手段,揭示了精神应激下微生物失调驱动肠干细胞分化异常的信号分子及其机制,为后续开展脑肠轴信号传递、靶标发现及药物精准干预研究提供了新思路与潜在新靶点。该研究工作受到国家重点研发计划、国家自然科学基金创新研究群体项目、国家高层次青年人才计划、我校兴药学者计划等资助,得到靶标天然药物全国重点实验室及江苏省药物代谢动力学重点实验室等平台的大力支持。
原文链接:https://www.cell.com/cell-metabolism/fulltext/S1550-4131(23)00477-1
Nature官网报道链接:https://www.nature.com/articles/d41586-024-00188-4
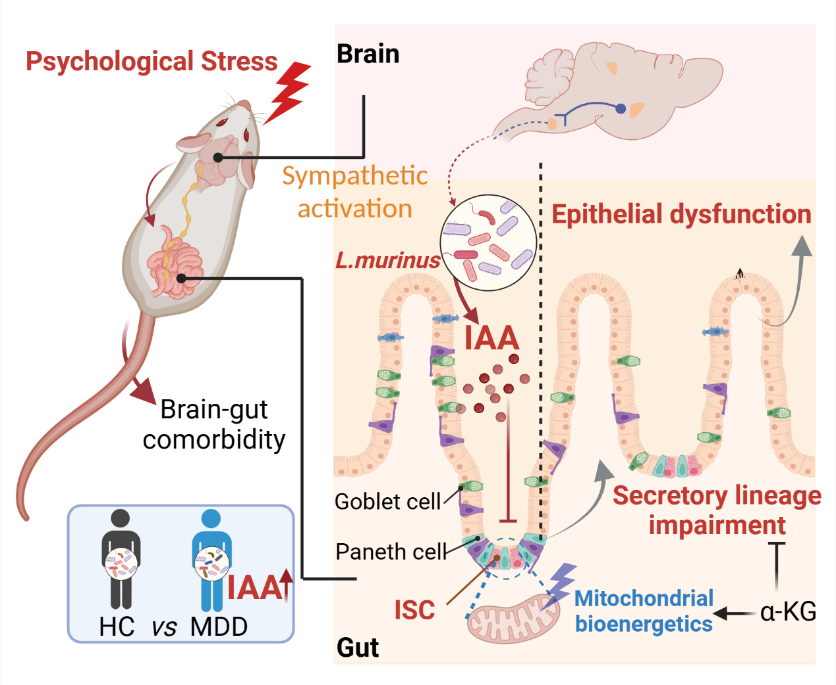
示意图
(供稿单位:3499cc拉斯维加斯入口,撰写人:刘华)





